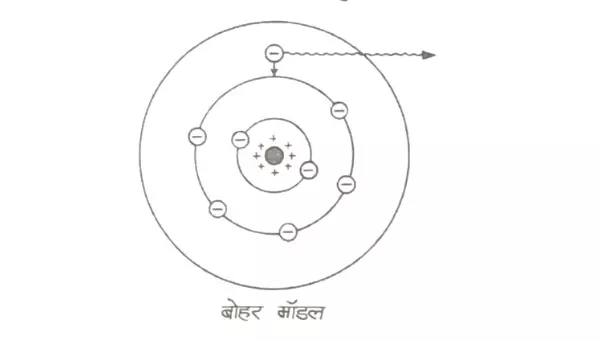
सन् 1913 में प्रो० नील बोहर (Niel Bohr) ने रदरफोर्ड के परमाणु मॉडल में मैक्स प्लांक के क्वाण्टम सिद्धान्त (quantum theory) को
लगाकर रदरफोर्ड मॉडल की कमियों को दूर कर दिया। इसके लिये उन्होंने निम्नलिखित तीन नयी परिकल्पनाएँ अथवा अभिग्रहीत (postulates) प्रस्तुत की :
बोहर का परमाणु मॉडल
(i) इलेक्ट्रॉन ‘केवल’ उन्हीं कक्षाओं में घूम सकते हैं जिनमें उनका कोणीय संवेग (angular momentum) h/2 π का पूर्ण गुणज हो, जहाँ h प्लांक का सार्वत्रिक नियतांक (Planck’s universal constant) है। यदि इलेक्ट्रॉन का द्रव्यमान m हो तथा वह r त्रिज्या की कक्षा में v वेग से घूम रहा हो, तो उसका कोणीय संवेग m v r होगा। बोहर की इस परिकल्पना के अनुसार, (Bor ka parmanu model in hindi).
mvr = nh/2π
जहाँ n एक पूर्णांक है (n = 1, 2, 3, …) जिसे कक्षा की ‘क्रम संख्या‘ अथवा ‘मुख्य क्वाण्टम संख्या‘ (principal quantum number) कहते हैं। इस समीकरण को ‘बोहर का क्वाण्टीकरण प्रतिबन्ध’ (Bohr’s quantisation condition) कहते हैं। इस प्रकार, परमाणु के बोहर मॉडल में इलेक्ट्रॉन केवल कुछ ‘निश्चित’ त्रिज्याओं वाली कक्षाओं में ही घूम सकते हैं, सभी में नहीं। इन कक्षाओं को ‘स्थायी कक्षाएँ‘ (stable orbits or stationary orbits) कहते हैं।
(ii) स्थायी कक्षाओं में घूमते समय इलेक्ट्रॉन ऊर्जा का उत्सर्जन ‘नहीं’ करते, यद्यपि उनमें अभिकेन्द्र त्वरण होता है। अत: परमाणु का स्थायित्व बना रहता है।
(iii) जब परमाणु को किसी कारणवश बाहर से ऊर्जा मिलती है, तो उसका कोई इलेक्ट्रॉन अपनी निश्चित कक्षा को छोड़कर किसी ऊँची कक्षा में चला जाता है। परमाणु की यह अवस्था ‘उत्तेजित‘ अवस्था (excited state) कहलाती है। इलेक्ट्रॉन ऊँची कक्षा में केवल 108 सेकण्ड के लिए ठहरकर, तुरन्त नीची कक्षा में वापस लौटता है तथा लौटते समय विद्युतचुम्बकीय तरंगों के रूप में ऊर्जा उत्सर्जित करता है।
यदि ऊँची कक्षा में इलेक्ट्रॉन की ऊर्जा E2 हो तथा नीची कक्षा में E] हो, तो उत्सर्जित तरंगों की आवृत्ति v निम्नलिखित समीकरण के अनुसार होती है.
h v = E2 – E1
अथवा v = E2 – E1 / h
इस समीकरण को ‘बोहर का आवृत्ति प्रतिबन्ध‘ (Bohr’s frequency condition) कहते हैं। परमाणु से ऊर्जा का उत्सर्जन केवल तभी होता है जब कोई इलेक्ट्रॉन किसी निश्चित ऊँची कक्षा से निश्चित नीची कक्षा में लौटता है। अत: किसी परमाणु से केवल कुछ निश्चित आवृत्तियों की ही तरंगें उत्सर्जित होती हैं जिनके कारण रेखिल स्पेक्ट्रम (line spectrum) प्राप्त होता है जिसमें तीक्ष्ण रेखाएँ (sharp lines) होती हैं। Bor model in hindi.
इसके आधार पर हाइड्रोजन के स्पेक्ट्रम की सफल व्याख्या की गई। परमाणु का बोहर मॉडल आधुनिक भौतिकी की आधार शिला है तथा इसके लिये बोहर को सन् 1922 में नोबेल पुरस्कार प्रदान किया गया। बाद में बोहर के मॉडल में सॉमरफिल्ड (Sommerfeld) तथा दी-ब्रोगली (de-Broglie) ने अनेक सुधार किये।